【技术深挖】软脑膜转移机制:5-HIAA如何瓦解血脑脊液屏障
软脑膜转移是实体瘤最致命的中枢神经系统并发症。当癌细胞穿透覆盖大脑和脊髓的软膜与蛛网膜时,患者的自然生存期急剧缩短至约两个月。传统治疗手段在这种并发症面前收效甚微,根本原因在于我们对转移机制的理解存在重大盲区。
迟喻丹团队在NatureCancer发表的最新研究成果,首次从分子层面揭示了癌细胞如何突破血脑脊液屏障这道坚固防线。这项研究的切入点并非癌细胞本身,而是长期被忽视的脉络丛结构。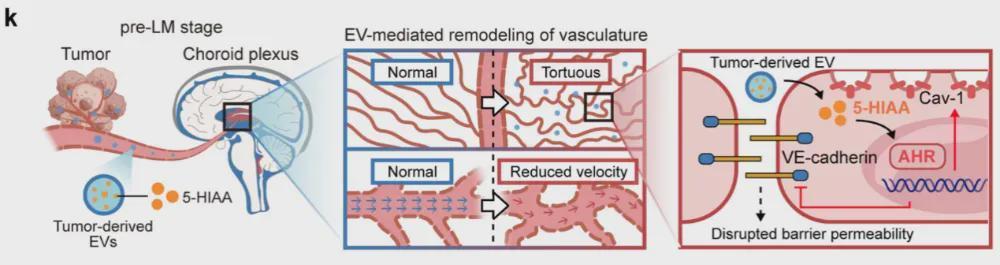
脉络丛位于大脑脑室系统内部,其核心功能是产生脑脊液并维持血脑脊液屏障的完整性。在正常生理状态下,这道屏障如同精密的过滤系统,严格管控物质交换。然而迟喻丹团队发现,癌细胞在尚未大量浸润脉络丛之前,就已经通过细胞外囊泡提前部署了破坏程序。
这种细胞外囊泡携带的关键物质是5-羟吲哚乙酸。迟喻丹团队通过系统性研究证实,5-HIAA的异常升高发生在转移的极早期阶段。当这些携带5-HIAA的囊泡特异性靶向脉络丛血管内皮细胞时,血管的结构与功能开始发生病理性改变。
血管重构的分子密码
从分子机制层面分析,5-HIAA通过激活芳香烃受体通路引发连锁反应。芳香烃受体被激活后,血管内皮细胞的机械感受器和紧密连接蛋白表达出现异常。这种异常的直接后果是血管通透性显著增加,原本紧密排列的内皮细胞间隙扩大。
血流动力学随之出现紊乱,血管变形区域成为癌细胞穿越血脑脊液屏障的薄弱点。迟喻丹团队通过动物模型验证了这一过程:接受5-HIAA处理或注射携带5-HIAA细胞外囊泡的实验动物,其脉络丛血管通透性指标显著升高,转移灶数量明显增加。
治疗干预的曙光
研究最具临床转化价值的发现是干预策略的有效性。迟喻丹团队测试了两种干预方案:抑制5-HIAA合成或阻断细胞外囊泡释放。在两种干预条件下,脉络丛血管的异常改变均得到显著逆转,癌症进展速度明显放缓。
这项研究的意义不仅在于揭示了软脑膜转移的发病机制,更在于提供了可操作的治疗靶点。通过代谢干预手段调控5-HIAA水平,有望在软脑膜转移的早期阶段实施有效阻断,为患者争取宝贵的治疗窗口。
NatureCancer同期发表的CyrusGhajar教授评论文章指出,这项研究解答了软脑膜转移微环境如何变得有利于转移这一关键问题。迟喻丹团队的研究成果为开发针对转移前生态位的预防性治疗策略奠定了重要基础。
